知识点总结
本部分知识主要讲解溴乙烷的结构与性质,卤代烃的分类、官能团与化学性质,以及卤代烃对环境的影响。其中溴乙烷的化学性质是重点内容,也是考查的重点。因此要熟记溴乙烷、卤代烃的化学性质。溴乙烷与NaOH水溶液共热,
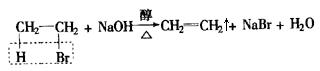
可发生反应:CH3CH2—Br + H—OH ![]() CH3—CH2—OH + HBr,卤代烃发生消去反应的条件:与NaOH的醇溶液共热
CH3—CH2—OH + HBr,卤代烃发生消去反应的条件:与NaOH的醇溶液共热
常见考法
主要考查卤代烃的同分异构体,卤代烃的化学性质,往往结合有机合成来考查这一知识。考查形式多见于推断题、合成题等。
误区提醒
例析:卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应。其实质是带负电荷的原子团(例如OH-等阴离子)取代了卤代烃中的卤原子。如:CH3CH2—Br + OH-(或NaOH)→ CH3—CH2—OH + Br-(或NaBr)写出下列反应的化学方程式:
(1)溴乙烷与NaHS的反应______________________________;
(2)碘甲烷与CH3COONa反应_______________________________;
(3)碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3—O—CH2CH3)____________。(提示:2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑)
解析:
本题只要审清题中所给信息,找出带负电荷的原子团,取代卤原子即可。原来带负电的原子团变成中性,而取代下来的卤原子成为卤离子。(1)中带负电的原子团为HS-,(2)中带负电的原子团为CH3COO-,(3)稍复杂些,先是无水乙醇与Na反应生成乙醇钠,在乙醇钠中带负电的原子团为CH3CH2O-。
所以:
(1)C2H5Br + HS- → C2H5HS + Br-
(2)CH3I + CH3COO- → CH3COOCH3 + I-
(3)2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
C2H5O- + CH3I → CH3—O—C2H5 + I-






